Forschungsschwerpunkte
Der Schwerpunkt meiner Gruppe liegt auf der Analyse des Zusammenhangs zwischen Interchromatinraum, Chromatin und Transkription, und der Frage, wie die zugrunde liegenden molekularen Mechanismen die Stressreaktion bei altersbedingten Prozessen und Neurodegeneration koordinieren. Unsere Arbeit hat vielfältige Auswirkungen, die vom Verständnis der Krankheitsursache bis hin zur Identifizierung von arzneimitteltauglichen Molekülen reichen. Unsere Studien beinhalten Mausmodelle, Patientenmaterial und modernste (Epi-)Genomik, wobei letztere durch einen starken Kern an Bioinformatik unterstützt wird.
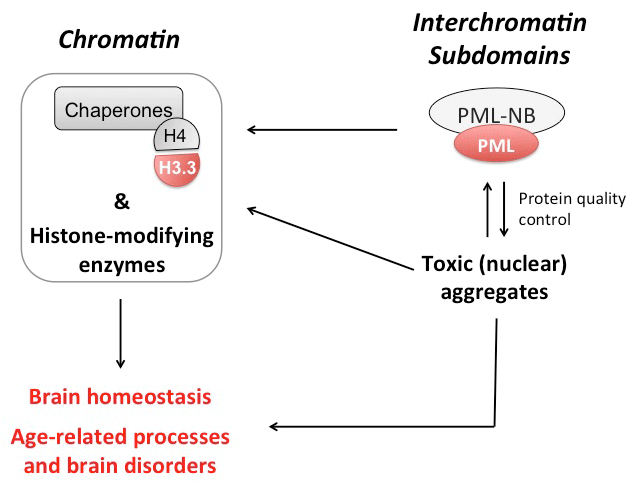
Der PML-Kernkörper in der Hirn-Homöostase und Stressreaktion. PML – das Promyelozytenleukämie Protein - ist der wesentliche Bestandteil einer im Zellkern befindlichen Struktur des Interchromatinraums, so genannte PML-Kernkörper (PML-nuclear body, PML-NB), die in die Kontrolle der Zelltypentwicklung unter physiologischen Bedingungen und bei Stress involviert sind. PML reguliert die Stammzellentwicklung während der Gehirnentwicklung (Regad et al, Nat Neurosci 2009), mit möglichen Auswirkungen auf kognitive Funktionen und Verhalten. Darüber hinaus kontrolliert PML die Zellmigration während der Neurogenese durch epigenetische Kontrolle der axonalen Lenkungsgene (Amodeo, A et al, Cell Rep 2017). PML unterdrückt Transkription durch Regulation der Proteinmenge der Komponenten des Polycomb repressiv complex 2. Da PML die Proteostase falsch gefalteter Proteine und den Schutz vor Neurodegeneration vermittelt, untersuchen wir die Aufgabe von PML bei der Qualitätskontrolle und Stabilität von im Zellkern befindlichen Proteinen in Neuronen mit einem besonderen Fokus auf Chromatin verändernden Komplexen (siehe unten) unter normalen physiologischen Bedingungen und in neurodegenerativen Krankheitsmodellen.
Epigenetische Kontrolle bei Auftreten und Fortschreiten von altersbedingten Veränderungen/Pathologien
Die mit PML-interagierenden Proteine DAXX und ATRX vermitteln die Beladung der Histon- Variante H3.3, die bei postmitotischen Zellen aufgrund ihrer replikationsunabhängigen Chromatinbeladung eine entscheidende Rolle spielt. Wir haben gezeigt, dass die Calcium-Signalwechselwirkung nach neuronaler Aktivierung die H3.3-Beladung fördert, was zu einer Veränderung der Chromatinstruktur und der Transkription im ZNS führt (Michod et al, Neuron 2012). Dies hat Auswirkungen auf die neuronale Plastizität, depressives Verhalten und den Alterungsprozess. In diesem Zusammenhang hat Daniele Banos Gruppe (DZNE Bonn) in Zusammenarbeit mit uns festgestellt, dass die Beladung von H3.3 in Prozessen zur Verlängerung der Lebensdauer auf organismischer Ebene eine Rolle spielt (Piazzesi et al, Cell Rep 2017). Zusätzlich finden sich Treiber-Mutationen in H3.3, sowie in ATRX und DAXX bei Hirntumoren. Daher ist H3.3 ein facettenreicher Faktor am Scheideweg der Plastizität des Gehirns, altersbedingter Funktionsstörungen und neoplastischer Hirnerkrankungen.
Wir untersuchen nun die Rolle der H3.3-Beladung und der damit verbundenen Histon-modifizierenden Enzyme (sowie der PML-NBs, siehe oben) bei der Koordination stereotypischer Stressreaktionswege, dem Alterungsprozess und des Auftretens/Fortschreitens neurodegenerativer Erkrankungen. Im Rahmen unserer translatorischen Bemühungen führen wir High-Content-Screenings durch, um Moleküle zu identifizieren, die die Histon-Variantenbeladung sowohl bei physiologischen als auch bei pathologischen Bedingungen modulieren.
Letztlich hat die ERC-geförderte Arbeit in unserem Labor zur Generierung eines krankheitsbildgetreuen somatischen Modells der von mutiertem H3.3 gesteuerten Tumorentstehung geführt, das Einblicke in die Krankheitsmechanismen gewährt (Pathania et al, Cancer Cell 2017; F1000). Unsere Erfahrung in der Modellierung und Erforschung von Chromatin-assoziierten Signalwegen, die neoplastischen Erkrankungen zugrunde liegen, versetzt unsere Gruppe in die einzigartige Lage, die epigenetische Umprogrammierung bei altersbedingten Hirnstörungen und Hirntumoren zu vergleichen und bietet uns die Möglichkeit mögliche gemeinsame Mechanismen zu identifizieren.